Àcua
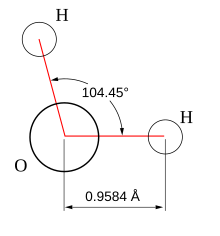
L'acua (dita anca lensa o agua), in condision de tenperadura e presion standard, la xe un licuido senxa color, senxa saor e senxa odor, co un punto de fuxion a 0 °C e un punto d'ebolision a 100 °C. La so molecola la xe formà da un atomo de osixeno dove che xe ligai do atomi de idroxeno; la so formula chimega la xe cuindi H2O.
| Àcua | |
 | |
| Sostansa chìmega | type of chemical entity |
|---|---|
| Masa | 18,011 u |
| Fòrmuła bruta o mołecołare | H2O |
| Faxesto da | |
| Fuxion | 0°C |
| Nùmaro CAS | |
| Nùmaro EINECS | 231-791-2 |
| Còdaze ATC | Errore script: la funzione "arraytostring" non esiste. |
| PubChem | 962 e 22247451 |
| DrugBank | DBDB09145 |
| SMILES | O |

Al stao sołido la xe ciama jaso e la ghe someja al viero. Al so stao gasoxo invece la xe nota cofà vapor acueo o pì senplicemente come vapor.
Al de sora de certi valori de tenperadura e presion (ciamai criteghi), che par l'acua i xe 647 K e 22,064 × 106 pascal, l'acua la va drento un stao dito supercritego, ndo' che i agregai de acua al stao simi-licuido i fluixe in na fase de simi-vapor.
La se trova in gran parte de l'Universo, come inte la Luna e in altri pianedi. Su la Tera l'acua coerse el 70,8% de la superfixe del pianeda.
El volume de acua prexente inte la Tera el xe stimà in 1 360 000 000 km³. Se trova inte:
Etimoloxia
canbiaEl termine "acua" el ga orixine dal latin aqua che vien ricondoto a la radice indoeuropea ak- co el signifigà de piegar (che xe prexente inte el sanscrito ak-na, piegà, cofà anca in altre lengue)[1], talvolta co un scanbio de soni intrà c, p e f (cfr. el sanscrito ap, el xendo afs, l'itita akwanzi "lori i beve", e el lituan uppe "un fiume").
Fìxica e chìmega de ł'acua
canbiaŁe prime scoerte sientifighe
canbiaŁa convinxion che l'acua fuse un ełemènto primixenio e indivixìbiłe se ga protato fin inte i ultemi dexeni del XVIII secoło, cuando i siensiài Antoine Lavoisier e Henry Cavendish i ga descoerto che sta sostansa ła xe formà in realtà da do costituènti: idroxeno e osìgeno. Inte el 1742, Anders Celsius el ga definìo ła scała de tenperatura che porta el so nome, ponendo el ponto de fuxion del'aqua (a ła normałe presion atmosferega) a 0 gradi e el ponto de ebołision a 100 gradi[2]. Ła prima sconpoxision del'aqua in idroxeno e osìgeno (i so conponènti ełementari) ze stà exeguìa inte el 1800 dal chimego inglexe William Nicholson, tramide el proceso de eletrołisi del'aqua.[3] L'aqua xe infati parsialmènte disocià in ioni H+ e OH-, che i migra verso i do połi de ła sela eletrołitiga, andove che se verifega łe seguènti reasion:
- anodo (+): 4 OH- → O2 + 2 H2O + 4 e-
- catodo (−): 2 H+ + 2 e− → H2
l'osìgeno e l'idroxeno i xe produzesti soto forma de bołe gasoxe su ła superfise dei eletrodi, da ndo' che i pol esar rancurài. Gilbert Newton Lewis el ga ixołà el primo canpion de pura aqua pexante (andove l'idroxeno xe sostituìo dal deuterio, só ixotopo) inte el 1933.[4]
Na controversia scientifega xe nada a ła fin dei ani sesanta a propoxito del'existensa de na forma połimerega del'aqua (ła połiaqua). Xe ora mai condivixa l'opinion che tałe połiaqua nó ła exista. [5][6][7] Inte el 2007 grasie al'uxo de superconputer e a ła mecanega cuantistiga xe stà sviłupà un modèło numerego del'aqua che a partir da i prinsipi de ła mecanega cuantistiga de łe mołecołe ghe ne estrapoła el conportamènto in modo coreto.[8]
I canbiamènti de stato de l'acua
canbiaL'acua ła xe una de łe pì picenine tra łe sostanse existenti (insiem a galio, bismuto e antimonio) andove el proceso de sołidificasion avien co un aumento de vołume spesifego (pari a sirca 0,087 L/kg, a ła tenperadura de 0 °C (273,15 K) a ła presion de 1 atm), mèntre el so ponto de ebołision el xe a 100 °C (373,15 K).[9] Cuèsto conporta che a ła diminusion de ła tenperadura, ła presion corispondènte al pasajio de stato sołido-licuido aumènti sensibilmènte: se ga na pendensa negadiva de ła linea de pasajio sołido-licuido inte el diagrama de faxe presion-tenperadura. In particołar, par ogni senteximo de grado Celsius (0,01 °C) de diminusion de ła tenperadura se ga un aumento de ła presion de fuxion de sirca na atmosfera. Sta relasion ła se verifega fin a ła presion de 2070 atm e a ła tenperadura de -22 °C, oltra se ga altri stati ałotropisi.
A ła presion atmosferega (1 atm) l'aqua ła boje a ła tenperadura de 100 °C. Cofà par tute łe altre sostanse, dorante ła trasformasion cogna fornir na serta cuantità de całor (deto całor latènte), che inte el caxo del'aqua el xe pì ełevà de ogni altra sostansa nota: a condision de 0 °C e de 1 atm cuesto całor de vaporixasion el xe infati pari a 2501 kJ/kg.
Fra i 90 °C e i 250 °C vałe ła regoła enpirega che ła presion de vaporixasion (in bar) ła xe pari a ła cuàrta potensa de ła sentesima parte de ła tenperadura de vaporixasion (in gradi Celsius):
Ła natura anfòtera de l'acua
canbiaL'acua ła xe anca na sostansa anfòtera, o sia bona de conportarse sia da açido che da baxe (chìmega).
A pH 7 (condision de neutrałità) ła consentrasion de ioni idrosido OH- xe uguałe a cuèła de ioni idroxeno H+ (o idronio o osonio H3O+). Cò cuesto equiłibrio el vien alterà, ła sołusion ła se trasforma in açida (majior consentrasion de ioni idroxeno) o baxiga (majior consentrasion de ioni idrosido).
Secondo ła tèoria de Brønsted-Lowry, un açido el xe na spese chìmega bona de donar un ione H+ e na baxe xe na spese chìmega bona de adisionarlo a sé. In prexensa de un açido pì forte de eła, l'aqua ła se conporta da baxe, in prexensa de un açido pì debołe de eła, l'aqua ła se conporta da açido. Par exenpio, inte el equiłibrio:
- HCl + H2O ⇄ H3O+ + Cl-
l'aqua ła se conporta cofà baxe e un açido łe dona el so ione H+. Invese inte ła reasion co l'amoniaga:
- NH3 + H2O ⇄ NH4+ + OH-
ła xe l'aqua a azir da açido, donàndoghe el so ione H+ a st'ultema.
El ione H3O+, prexente senpre in cuantità picenine insieme a ła normałe mołecoła d'aqua, se forma dopo a ła reasion chìmega de autoprotołixi del'aqua:[10]
- 2H2O ⇄ H3O+ + OH-
Sta reasion ła xe anca nota cofà autoionixasion,[11] semi-ionixasion o autodisociasion del'aqua, e spiega ła natura anfòtera del'aqua.
L'inportanza biołoxica de l'acua
canbiaL'acua ła xe na conponènte fondamentałe de tuti i organismi vivènti prexenti su'l nostro pianeda. Ła se cata in ełevate persentuałi un te łe celule (in particołar inte el sitoplasma e inte i vacuołi – prexenti inte łe celule vexetałi e in on fià de protisti), indove al' interno vien convojià 'traverso el proceso de pinocitoxi.[13] Inte el protoplaxma de tute łe celule, sia procarioti sia eucarioti, l'aqua raprexenta el conposto predominante e ła agise cofà solvente par tute łe biomołecołe (cofà i carboidrati, łe proteine, łe vitamine idrosołubiłi ecc.), dàndoghe ła posibiłità de reagir tra de łore un te łe varie reasion biochìmighe. Oltre che cofà solvente, l'aqua partesipa ativamènte anca cofà reaxente in diverse reasion metabołiche, soratuto cuèłe de idrołisi e ła xe, asieme a l'anidride carbonega, uno dei prinsipałi reaxenti de ła fotosintexi clorofijana; xe anca, senpre asieme a ła CO2, el prodoto concluxivo del proceso de respirasion selułar.
Esendo el prinsipałe costituènte de ła gran parte dei viventi, l'aqua xe donca prexente anca inte el organixmo uman, in persentuałi variabiłi a seconda de l'età, del seso e del pexo. I fluidi corporei che i ga el majior contenuo de aqua xe el licuido cefało-rachidian (99%), el midoło oseo (99%) e el plasma sanguigno (85%).[14][15] Ła rixulta cuindi de fondamentałe inportansa par el trasporto dei nutrienti in tuti i distreti corporei e par l'eliminasion e l'escresion, tramide l'urina, de łe scorie prodote inte łe reasion biochìmighe. L'aqua ła svolge anca na funsion de granda inportansa inte ła regołasion de ła tenperadura corporea (tramide ła sudorasion) e de ła consentrasion dei sałi minerałi; partesipa anca a ła digestion, faorèndo el tranxito intestinałe e l'asorbimènto de łe sostanse nutridive. Propio parché l'aqua ła ga da esar prexente in cuantità asè elevàe inte ła alimentasion umana ła vien clasifegà cofà "macronutriente".[16]
Inte łe piante ła xe el conponènte prinsipałe de ła linfa, che ła ga ła funsion de trasportar i prinsipi nutritivi in tuti i tesuti, e dei vacuołi, che i regoła ła presion osmotega.
Uxi de l'acua
canbiaL'aqua ła riveste un roło sentrałe in un grando numaro de canpi. Sostansialmènte se pol sudividare i uxi del'aqua in:
- Uxi siviłi:
- Uxo potabiłe
- Ałimentasion (preparasion de łe cose da magnar e da bevare)
- Ixene (personałe e dei inpianti sanidari)
- Inprexe ałimentari
- Uxi siviłi nò potabiłi (par tanti de cuesti, comunque, se uxa de norma aqua potabiłe), intrà cui:
- Uxo potabiłe
- Uxi agricołi (irigasion)
- Utiłixi industriałi, intrà cui:[17]
- Fonte enerxetica in inpianti idroełetrisi
- Aplicasion chìmighe (cofà solvente e azente de reasion)
- Vetor termego in inpianti de riscaldamènto e rafredamènto.
Anca se l'aqua recoerxe el 71% de ła superfise terestre, ła majior parte de cuesta nò ła xe utiłixàbiłe diretamènte, in cuànto nesesita de particołari tratamènti, che i xe difarenti ficài a seconda de l'utiłixo che l'aqua ła xe destinà.
Proverbi
canbia- Quando che l'acua toca el cuło, tuti inpara a noare vol dir " quando ghe xe davero na urgensa, tuti se se dà na mosa e se se tira fora da łe rogne ".
- Chi che se ga scotà co l'acua calda, el ga paura anca de queła freda vol dir " quando uno ga avudo na bruta esperiensa co un problema grando, el ga paura anca dei problemi pì picołi".
- L'acua ronpe dove che no se crede vol dir " ocio ai tipi cheti che no se rabia mai: xe proprio questi che, quando i se sbroca, e no te te ło speti, i diventa na furia, come na brentana".
Notasion
canbia- ↑ Termine exato
- ↑ Celsius, op. cit.
- ↑ Nicholson, op. cit.
- ↑ (EN) Gilbert N. Lewis, The isotope of hydrogen, in Journal of the American Chemical Society, vol. 55, nº 3, marso 1933, pp. 1297–1298, DOI:10.1021/ja01330a511. entrada il 14-08-2009.
- ↑ (EN) Denis Rousseau, Case Studies in Pathological Science, in American Scientist, vol. 80, nº 1, zenaro 1992, pp. 54–63. entrada il 14-08-2009.
- ↑ (EN) Henry H. Bauer, "Pathological Science" is not Scientific Misconduct (nor is it pathological), in International Journal for Philosophy of Chemistry, vol. 8, nº 1, 2002, pp. 5-20. entrada il 14-08-2009.
- ↑ (EN) Felix Franks, David Eisenberg, A Scientific Gold Rush. (Book Reviews: Polywater), in Science, vol. 213, nº 4512, settembre 1981, pp. 1104-1105. entrada il 14-08-2009.
- ↑ I segrèti del'aqua, in Łe Sciense, 6 marzo, 2007. entrada il 14-08-2009.
- ↑ I ponti de fuxion e ebołision riportai i son riferìi a ła presion de 1 atm.
- ↑ Lausarot, op. cit.
- ↑ Brandi, op. cit.
- ↑ www.medicinaecologica.itmedicinaecologica.it.
- ↑ Funsion biołoxica de l'aqua (PDF)chimica-cannizzaro.it.
- ↑ El corpo uman e l'aquaecoline-fo.com.
- ↑ El roło del'aqua un te'l organixmodoctor33.it.
- ↑ I macronutriènti - L'aqua, el nutriente pì inportanteguide.supereva.it.
- ↑ Polizzotti, op. cit., p. 53.
Varda anca
canbia- Idrogeno
- Uxi de l'acua (Industriałe, pa' l'Agricoltura)
- Wikimedia Commons el detien imàjini o altri file so àcua
- el detien schemi gràfeghi so
| Controło de autorità | LCCN (EN) sh85145447 · GND (DE) 4064689-0 · BNF (FR) cb11931913j (data) · BNE (ES) XX524789 (data) · NDL (EN, JA) 00567741 |
|---|